La enfermedad hepática relacionada con el alcohol (ALD, por sus siglas en inglés) es un espectro de trastornos hepáticos que comienza con esteatosis, una etapa reversible de la enfermedad que puede progresar a cirrosis y cáncer de hígado. A pesar de ser una de las principales causas de enfermedad hepática crónica y morbilidad en el mundo, la patogenia de la ALD aún no se conoce por completo, lo que ha limitado la disponibilidad de terapias efectivas. Las características anatómicas y la complejidad funcional de la expresión génica en cada zona del acino hepático dificultan aún más la comprensión de los mecanismos por los que la ingesta crónica de alcohol lesiona los hepatocitos y los sensibiliza a la progresión hacia estadios más avanzados de la enfermedad.
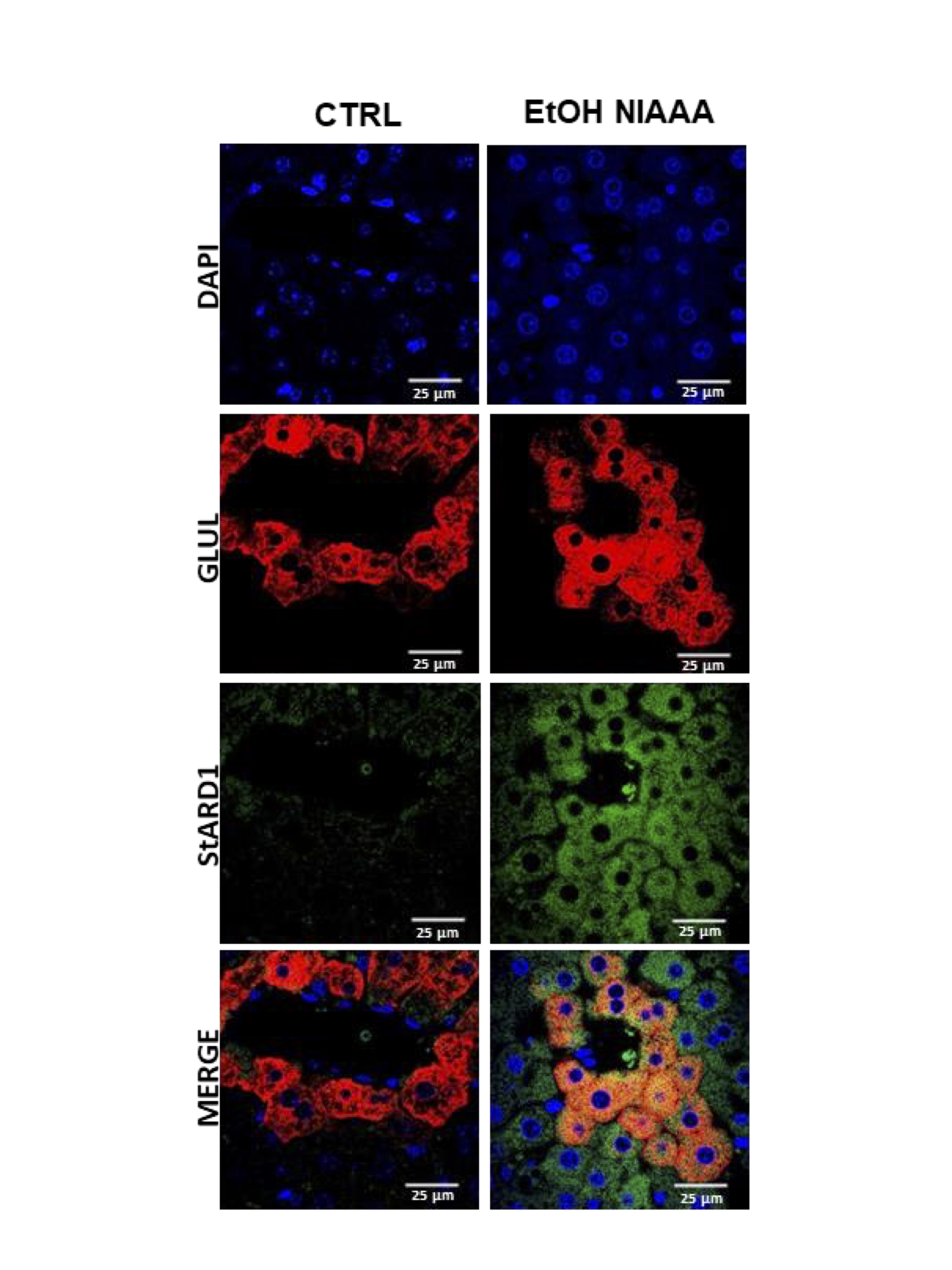
En un estudio reciente publicado en Journal of Lipid Research, el grupo de "Regulación mitocondrial de la muerte celular" revela que StARD1, una proteína de la membrana externa mitocondrial que transporta colesterol a la membrana interna mitocondrial para su metabolismo, se expresa predominantemente en la zona perivenosa (PV) en secciones del hígado de ratones alimentados crónicamente con alcohol. La distribución zonal de StARD1 se observa en etapas tempranas tras el tratamiento con dieta alcohólica (10 días) en hepatocitos asilados de la zona PV en comparación con hepatocitos de la zona periportal (PP). Esta expresión zonal de StARD1 induce la acumulación de colesterol en las mitocondrias y un aumento fr la peroxidación lipídica en los hepatocitos PV de ratones alimentados con alcohol en comparación con los hepatocitos PP. Análisis de microscopía electrónica de transmisión muestra unas alteraciones estructurales de la mitocondria particularmente de la zona PV. La determinación de la función mitocondrial mediante el consumo de oxígeno a tiempo real por tecnología de Seahorse revela una menor respiración máxima y una capacidad respiratoria preservada en los hepatocitos PV de ratones control, efectos que se revierten tras el tratamiento con la dieta alcohólica. Más importante aún, la diferencia tanto en la morfología como la actividad funcional de las mitocondrias entre los hepatocitos PP y PV después de la alimentación con alcohol es controlada por StARD1, ya que los ratones con deleción de StARD1 específicamente en hepatocitos (Stard1Δhep) son resistentes a los defectos funcionales y ultraestructurales de la mitocondria inducidos por el alcohol. Por lo tanto, este estudio identifica un factor adicional que puede contribuir a la sensibilidad zonal del hígado a los efectos perjudiciales del consumo crónico de alcohol además del conocido metabolismo preferente del alcohol en el área centrolobulillar. Varios factores convergen en esta área, tanto la menor tensión de oxígeno en esta zona y una mayor tasa de metabolismo del alcohol que interactúan para inducir StARD1, lo que conduce a un mayor flujo de colesterol a la mitocondria que incide en la función y la defensa antioxidante mitocondrial. Dichos hallazgos por tanto sugieren que StARD1 puede ser una nueva diana terapéutica en el tratamiento de la ALD.
Link del articulo: Fucho et al. Zonal expression of STARD1 and oxidative stress in alcoholic-related liver disease. doi: https://doi.org/10.1016/j.jlr.2023.100413.